Sự thoái hoá thần kinh và bệnh alzheimer
Từ khóa: Già hóa dân số; thoái hóa thần kinh; suy giảm nhận thức; người cao tuổi; chất lượng cuộc sống.
Neurodegeneration and Alzheimer's disease.
Summary: Population aging not only increases the need for chronic healthcare but also leads to a significant increase in neurodegenerative diseases, affecting cognitive function, motor skills, behavior, and quality of life in older adults.
Keywords: Population aging; neurodegeneration; cognitive decline; elderly people; quality of life.
Doi:
Ngày nhận bài: 22/11/2025
Ngày hoàn thiện biên tập: 29/10/2025
Ngày duyệt đăng: 10/01/2026
I. MỞ ĐẦU
Việt Nam đang bước vào giai đoạn già hóa dân số nhanh, với 14,2 triệu người từ 60 tuổi trở lên, chiếm khoảng 14% tổng dân số (Tổng cục Thống kê, 2025). Dự báo đến năm 2030, con số này sẽ tăng lên gần 18 triệu người, đưa Việt Nam tiến gần ngưỡng “dân số siêu già”. Già hóa dân số không chỉ làm tăng nhu cầu chăm sóc sức khỏe mạn tính mà còn kéo theo sự gia tăng đáng kể các bệnh lý thoái hóa thần kinh, gây ảnh hưởng đến chức năng nhận thức, vận động, hành vi và chất lượng cuộc sống của người cao tuổi.
Thoái hoá thần kinh là quá trình tiến triển đặc trưng bởi sự mất dần cấu trúc và chức năng của tế bào thần kinh, dẫn đến rối loạn dẫn truyền tín hiệu trong hệ thần kinh trung ương. Đây là hậu quả của sự tích tụ các protein bất thường (như amyloid, tau, α- synuclein), stress oxy hoá, rối loạn ty thể và phản ứng viêm mạn tính kéo dài trong mô não. Những thay đổi này diễn tiến âm thầm trong nhiều năm, gây suy giảm dần trí nhớ, khả năng tư duy, cảm xúc và hành vi — là nền tảng bệnh sinh của nhiều bệnh lý thoái hoá, trong đó có bệnh Alzheimer, nguyên nhân hàng đầu gây sa sút trí tuệ ở người cao tuổi.
Theo Tổ chức Y tế Thế giới (WHO, 2023), hiện có khoảng 55 triệu người mắc sa sút trí tuệ trên toàn cầu, trong đó 60–70% là do bệnh Alzheimer. Tại Việt Nam, ước tính có 500.000 - 600.000 người đang sống với căn bệnh này, và con số sẽ tiếp tục tăng cùng tốc độ già hoá dân số. Bệnh Alzheimer không chỉ gây suy giảm trí nhớ và khả năng nhận thức, mà còn dẫn đến rối loạn hành vi, mất khả năng tự chủ, và gánh nặng lớn về tâm lý, kinh tế đối với gia đình và xã hội.
Việc hiểu rõ quá trình thoái hoá thần kinh và bệnh Alzheimer không chỉ giúp nhận diện sớm các dấu hiệu suy giảm nhận thức mà còn tạo cơ sở cho việc bảo vệ sức khỏe não bộ và chủ động phòng ngừa sa sút trí tuệ thông qua lối sống lành mạnh và chăm sóc y tế định kỳ.
II. KHÁI NIỆM VÀ CƠ CHẾ CỦA QUÁ TRÌNH THOÁI HOÁ THẦN KINH
1. Khái niệm và đặc điểm chung
Thoái hoá thần kinh (Neurodegeneration) là thuật ngữ dùng để chỉ quá trình bệnh lý tiến triển, trong đó các tế bào thần kinh dần mất đi tính toàn vẹn về cấu trúc và chức năng trong hệ thần kinh trung ương, bao gồm cả não và tuỷ sống. Sự suy giảm này diễn ra có hệ thống, dẫn đến rối loạn hoạt động của mạng lưới dẫn truyền thần kinh, làm tổn hại khả năng duy trì cân bằng nội môi và điều hoà chức năng nhận thức – vận động của cơ thể.
Đây là cơ chế bệnh sinh cốt lõi của nhiều bệnh lý thần kinh mạn tính, như bệnh Alzheimer, Parkinson, Huntington, xơ cứng cột bên teo cơ (ALS)... Điểm đặc trưng của các bệnh này là sự chết tế bào thần kinh có chọn lọc, thường tập trung ở một số vùng chức năng nhất định, dẫn đến các biểu hiện lâm sàng tương ứng - ví dụ, hồi hải mã (hippocampus) trong bệnh Alzheimer, hay chất đen (substantia nigra) trong Parkinson.
Khác với tổn thương cấp tính như đột quỵ hay chấn thương sọ não, quá trình thoái hoá thần kinh diễn ra âm thầm, kéo dài và không hồi phục, thường bắt đầu hàng năm trước khi có biểu hiện triệu chứng lâm sàng. Cơ chế tiến triển chậm và đa yếu tố này khiến việc phát hiện sớm và điều trị đặc hiệu gặp nhiều thách thức.
2. Cơ chế của quá trình thoái hoá thần kinh
Thoái hoá thần kinh không phải là hậu quả của một cơ chế đơn lẻ, mà là kết quả của nhiều rối loạn sinh học cùng xảy ra và tương tác lẫn nhau trong tế bào thần kinh và môi trường xung quanh. Khi các cơ chế bảo vệ và phục hồi của tế bào bị suy yếu dưới tác động của tuổi tác, yếu tố di truyền hay môi trường, tế bào thần kinh dần mất đi tính toàn vẹn cấu trúc và chức năng, dẫn tới tổn thương lan tỏa và thoái hoá tiến triển.
2.1. Tích tụ protein bất thường
Một đặc điểm quan trọng của các bệnh thoái hoá thần kinh là sự gấp sai và tích tụ của protein bất thường trong tế bào thần kinh. Khi cơ chế phân huỷ tự nhiên bị rối loạn, các protein này không được loại bỏ qua hệ thống tiêu huỷ nội bào, dẫn đến hình thành những thể vùi không hoà tan cản trở hoạt động của tế bào.
Tuỳ từng bệnh, loại protein tích tụ sẽ khác nhau: amyloid-β và tau trong Alzheimer, α-synuclein trong Parkinson, TDP-43 và SOD1 trong ALS... Các lắng đọng này gây độc thông qua rối loạn màng tế bào, mất cân bằng ion, ức chế dẫn truyền tín hiệu và kích hoạt chết tế bào theo chương trình (apoptosis). Ngoài ra, các protein sai cấu trúc còn có khả năng lan truyền theo cơ chế “kiểu prion”, lây sang các tế bào lân cận qua synapse hoặc túi ngoại bào, khiến tổn thương lan rộng theo thời gian.
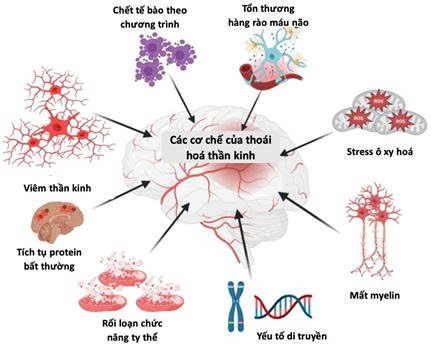 |
| Hình 1. Các cơ chế của quá trình thoái hoá thần kinh (Nguồn: Saikia , Dhanushkodi, 2024) |
2.2. Rối loạn chức năng ty thể và stress oxy hoá
Ty thể đóng vai trò trung tâm trong chuyển hoá năng lượng và kiểm soát sự sống của tế bào thần kinh. Khi chuỗi hô hấp bị rối loạn, tế bào giảm sản xuất ATP và tạo ra lượng lớn các gốc tự do oxy hoá (ROS), gây stress oxy hoá và tổn thương DNA, lipid màng và protein.
Trong bệnh Parkinson, đột biến các gen PINK1 và PRKN làm suy giảm quá trình loại bỏ ty thể hư hỏng (mitophagy), dẫn tới tích tụ ROS. Trong bệnh Alzheimer, Aβ gây rối loạn cân bằng hợp nhất – phân chia ty thể và làm gián đoạn vận chuyển năng lượng dọc sợi trục neuron. Stress oxy hoá không chỉ là hậu quả mà còn thúc đẩy thêm gấp nếp protein sai cấu trúc và phản ứng viêm thần kinh, hình thành vòng xoắn bệnh lý tự khuếch đại.
2.3. Phản ứng viêm thần kinh
Khi tế bào thần kinh bị tổn thương, các tế bào miễn dịch của não như tế bào thần kinh đệm nhỏ (microglia) và tế bào hình sao (astrocyte) sẽ được kích hoạt để dọn dẹp vùng tổn thương. Tuy nhiên, khi phản ứng này kéo dài, chúng giải phóng quá nhiều chất gây viêm như interleukin (IL-1β, IL-6) và yếu tố hoại tử u (TNF-α). Những chất này làm tổn thương thêm tế bào thần kinh khỏe mạnh và duy trì tình trạng viêm mạn tính trong não.
Một số nghiên cứu mới chỉ ra rằng tế bào gốc và các túi tiết của chúng có thể giúp điều chỉnh phản ứng viêm, làm giảm hoạt động gây độc và tăng khả năng bảo vệ thần kinh.
2.4. Suy giảm cơ chế tự thực bào và tiêu thể
Tế bào thần kinh có cơ chế “tự làm sạch” để loại bỏ những phần bị hư hại – được gọi là tự thực bào (autophagy) và tiêu thể (lysosome). Khi cơ chế này yếu đi, các chất thải và protein bất thường không được loại bỏ sẽ tích tụ lại, gây tắc nghẽn và rối loạn hoạt động của tế bào. Trong bệnh Alzheimer, sự suy giảm của hệ thống tự thực bào khiến mảng amyloid tích tụ nhanh hơn; trong Parkinson, đột biến một số gen làm giảm hoạt động của enzym trong tiêu thể, khiến thể Lewy hình thành. Sự suy yếu của quá trình này không chỉ làm tăng gánh nặng protein bất thường mà còn khiến tế bào thần kinh không thể phục hồi sau tổn thương.
Hiện nay, việc kích hoạt lại các cơ chế tự thực bào đang được nghiên cứu như một hướng mới giúp làm chậm tiến triển của bệnh.
2.5. Sự lan truyền bệnh lý theo kiểu prion
Trong những năm gần đây, nhiều nghiên cứu cho thấy các protein bị gấp sai cấu trúc trong não có khả năng “lây lan” sang các tế bào khác, theo cơ chế tương tự như prion – một loại protein gây bệnh đặc trưng trong bệnh bò điên (Creutzfeldt–Jakob ở người).
Bình thường, protein trong tế bào có cấu trúc ổn định và hoạt động đúng chức năng. Khi một protein bị gấp sai, nó có thể “ép” các protein bình thường xung quanh biến dạng theo, khiến quá trình gấp sai lan rộng dần. Các protein biến dạng này sau đó được vận chuyển ra ngoài tế bào thông qua các túi tiết nhỏ (exosome) hoặc qua các điểm tiếp xúc giữa tế bào thần kinh (synapse), rồi xâm nhập vào tế bào kế cận. Cơ chế “nhân bản và lan truyền” này giúp lý giải vì sao các bệnh thoái hoá thần kinh thường khởi phát khu trú ở một vùng não nhất định - chẳng hạn hồi hải mã trong Alzheimer hay chất đen trong
Parkinson — nhưng theo thời gian, tổn thương lại lan rộng dọc theo các đường dẫn truyền thần kinh liên quan đến trí nhớ, vận động và hành vi. Sự lan truyền theo kiểu prion khiến quá trình thoái hoá thần kinh diễn ra âm thầm, lan tỏa và khó đảo ngược.
2.6. Yếu tố di truyền và môi trường
Ngoài các cơ chế nội sinh, yếu tố di truyền và môi trường sống cũng quyết định phần lớn nguy cơ và tốc độ tiến triển của bệnh. Một số gen như APP, PSEN1, LRRK2, SNCA hoặc SOD1 khi bị đột biến sẽ làm rối loạn quá trình xử lý protein, chức năng ty thể hoặc phản ứng viêm.
Bên cạnh đó, tuổi cao, ô nhiễm, tiếp xúc với kim loại nặng, thuốc trừ sâu, chế độ ăn thiếu cân đối và ít vận động đều làm tăng stress oxy hoá và thúc đẩy tổn thương tế bào thần kinh.
Yếu tố di truyền tạo nên nền tảng dễ tổn thương, còn môi trường đóng vai trò kích hoạt hoặc làm nặng thêm quá trình thoái hoá. Chính sự kết hợp này khiến mỗi người có nguy cơ mắc bệnh và tốc độ tiến triển khác nhau, dù cùng sống trong một điều kiện tương tự.
3. Một số bệnh lý thoái hoá thần kinh
Các cơ chế bệnh sinh nêu trên là nền tảng chung của nhiều bệnh thoái hoá thần kinh. Tuy nhiên, mỗi bệnh có vị trí tổn thương, loại protein tích tụ và biểu hiện lâm sàng đặc trưng, tạo nên những hội chứng khác nhau.
3.1. Bệnh Alzheimer
Là nguyên nhân hàng đầu gây sa sút trí tuệ ở người cao tuổi, đặc trưng bởi mảng amyloid-β ngoài tế bào và rối sợi thần kinh do protein tau trong tế bào. Tổn thương tập trung ở hồi hải mã và vỏ não, khiến người bệnh dần mất trí nhớ, giảm tư duy và định hướng, tiến tới mất khả năng tự chăm sóc.
3.2. Bệnh Parkinson
Do thoái hoá tế bào thần kinh tiết dopamine ở vùng chất đen, gây run, chậm vận động, cứng cơ và mất thăng bằng. Mô bệnh học ghi nhận thể Lewy chứa α-synuclein gấp sai cấu trúc, là dấu ấn đặc trưng của bệnh.
3.3. Xơ cứng teo cơ một bên (ALS)
Là bệnh thoái hoá các tế bào vận động, khiến người bệnh yếu cơ, giật cơ và dần mất khả năng nói, nuốt, thở. Các protein liên quan gồm TDP-43, FUS và SOD1, gây tổn thương lan toả và tiến triển nhanh, hiện chưa có điều trị đặc hiệu.
3.4. Thoái hoá thùy trán – thái dương (FTD)
Tổn thương chủ yếu ở vùng kiểm soát hành vi và ngôn ngữ, dẫn đến thay đổi tính cách, hành vi không phù hợp và giảm ngôn ngữ. Bệnh liên quan đến protein tau hoặc TDP-43, thường khởi phát ở tuổi trung niên.
3.5. Sa sút trí tuệ thể Lewy
Có đặc điểm giao thoa giữa Alzheimer và Parkinson, với thể Lewy chứa α- synuclein trong nhiều vùng vỏ não. Người bệnh thường rối loạn chú ý, ảo giác thị giác và dao động nhận thức trong ngày, kèm các triệu chứng vận động tương tự Parkinson.
III. BỆNH ALZHEIMER
1. Đại cương
Bệnh Alzheimer là bệnh lý thoái hoá thần kinh tiến triển mạn tính, đặc trưng bởi suy giảm dần trí nhớ, tư duy, ngôn ngữ, hành vi và khả năng tự chủ, là nguyên nhân hàng đầu gây sa sút trí tuệ ở người cao tuổi, chiếm khoảng 60–70% tổng số trường hợp. Bệnh thường khởi phát sau 65 tuổi, tần suất mắc tăng rõ rệt theo tuổi, và được chia thành hai thể chính:
-
Thể khởi phát muộn (Late-Onset Alzheimer’s Disease – LOAD): chiếm đa số, liên quan nhiều đến yếu tố tuổi và gen APOE ε4.
-
Thể khởi phát sớm (Early-Onset Alzheimer’s Disease – EOAD): chiếm dưới 5% trường hợp, thường có yếu tố di truyền trội do đột biến các gen APP, PSEN1, PSEN2.
-
Trung bình, thời gian sống sau khi được chẩn đoán dao động từ 4–8 năm, có thể kéo dài đến hơn 10 năm tùy thuộc vào tuổi, tình trạng thể chất và mức độ chăm sóc.
2. Cơ chế bệnh sinh
Các thay đổi bệnh lý trong bệnh Alzheimer được đặc trưng bởi sự xuất hiện của hai protein bất thường: amyloid-β (Aβ) dạng mảng ở ngoại bào (plaque) và protein tau liên kết với vi ống bị phosphoryl hóa bất thường lắng đọng dưới dạng đám rối tơ thần kinh (neurofibrillary tangles).
- Mảng amyloid: Thành phần chính của mảng amyloid là protein Aβ. Protein bất thường này được tách ra từ protein amyloid tiền thân (amyloid precursor protein – APP) do enzyme β-secretase và γ-secretase tạo ra peptide Aβ40 và Aβ42. Aβ42 có tính kỵ nước cao, dễ kết tụ, tạo mảng amyloid gây độc thần kinh, kích hoạt viêm và stress oxy hoá.
- Đám rối tơ thần kinh: thành phần là các protein tau bị phosphoryl hoá quá mức, tách khỏi vi ống, kết tụ thành sợi xoắn kép, làm mất ổn định cấu trúc tế bào. Hai dạng tổn thương (mảng amyloid và đám rối tơ thần kinh) này thường thấy sớm ở hồi hải mã – trung tâm của trí nhớ, sau đó lan dần sang vỏ não đỉnh và trán, có liên quan đến sự xuất hiện và tiến triển tăng dần các triệu chứng lâm sàng của bệnh Alzheimer.
- Phản ứng viêm thần kinh: tế bào vi thần kinh đệm (microglia, astrocyte) được kích hoạt, tiết cytokine (IL-1β, TNF-α) gây tổn thương lan toả.
- Stress oxy hoá và rối loạn ty thể: giảm sản xuất ATP, tăng gốc tự do ROS, làm tổn thương DNA, lipid và protein tế bào.
- Yếu tố di truyền: đột biến gen APP, PSEN1, PSEN2 gây thể khởi phát sớm; kiểu gen APOE ε4 là yếu tố nguy cơ mạnh nhất của thể khởi phát muộn, làm giảm thanh thải Aβ.
- Yếu tố môi trường – lối sống: tuổi cao, ít vận động, trầm cảm, béo phì, tăng huyết áp, đái tháo đường và cô lập xã hội đều làm tăng nguy cơ khởi phát bệnh.
3. Triệu chứng lâm sàng
Bệnh Alzheimer điển hình khởi phát âm thầm, tiến triển chậm và biểu hiện nổi bật nhất bằng suy giảm trí nhớ. Trong các thể không điển hình, rối loạn ngôn ngữ, thị giác– không gian hoặc chức năng điều hành có thể xuất hiện sớm hơn.
3.1. Suy giảm trí nhớ (amnesia) Là triệu chứng chính và xuất hiện sớm nhất, thường được người thân phát hiện qua việc bệnh nhân quên các sự kiện mới, nhầm thời gian, để quên đồ vật. Suy giảm chủ yếu thuộc trí nhớ tình tiết (episodic memory) – trí nhớ về các sự kiện cá nhân, phụ thuộc vào vùng hồi hải mã và thùy thái dương trong, vốn bị tổn thương sớm trong cơ chế bệnh học.
Khi bệnh tiến triển, trí nhớ ngữ nghĩa (semantic memory) – hiểu biết về kiến thức và khái niệm chung – dần suy giảm, trong khi trí nhớ thủ tục (procedural memory) – kỹ năng vận động, thao tác – thường được bảo tồn cho đến giai đoạn muộn.
Trí nhớ gần suy giảm rõ rệt ở giai đoạn đầu, còn trí nhớ xa và trí nhớ tức thời tương đối được giữ. Về sau, suy giảm trí nhớ lan tỏa khiến bệnh nhân mất khả năng ghi nhớ và hồi tưởng toàn diện.
3.2. Mất ngôn ngữ (aphasia)
Rối loạn ngôn ngữ thường biểu hiện sớm bằng khó tìm từ, dùng từ không chính xác hoặc cấu trúc câu chưa hoàn chỉnh. Khi bệnh tiến triển, người bệnh nói lặp, giảm lưu loát, khó gọi tên đồ vật và có thể mất ngôn ngữ hoàn toàn ở giai đoạn nặng.
3.3. Mất sử dụng động tác (apraxia)
Là mất khả năng thực hiện các động tác đã biết dù chức năng vận động và cảm giác còn nguyên. Thường gặp mất dùng động tác ý niệm–vận động (ideomotor apraxia), bệnh nhân biết phải làm gì nhưng không thể bắt chước hoặc mô tả hành động (như động tác chải đầu). Tình trạng này gây khó khăn trong sinh hoạt: mặc quần áo, ăn uống, tự chăm sóc – là nguyên nhân chính dẫn đến mất khả năng tự lập và phụ thuộc người chăm sóc ở giai đoạn giữa – muộn.
3.4. Mất nhận thức (agnosia)
Bệnh nhân không thể nhận biết người, vật hoặc âm thanh dù cảm giác còn nguyên vẹn. Mất nhận thức thị giác không gian thường gặp nhất, do tổn thương vùng chẩm–thái dương trong, biểu hiện bằng mất nhận diện khuôn mặt (prosopagnosia) hoặc dấu hiệu gương – không nhận ra hình ảnh của chính mình.
3.5. Suy giảm chức năng điều hành
Khả năng lập kế hoạch, tổ chức, ra quyết định và xử lý thông tin giảm dần. Người bệnh khó thực hiện nhiều nhiệm vụ cùng lúc, mất khả năng làm việc độc lập và cần được giám sát trong sinh hoạt hàng ngày.
3.6. Giảm khả năng tự nhận thức (anosognosia)
Người bệnh thường không nhận ra sự suy giảm của bản thân, thậm chí phủ nhận triệu chứng. Khi khả năng tự nhận thức giảm, bệnh nhân dễ thực hiện các hành vi nguy hiểm như lái xe, nấu ăn. Mức độ anosognosia liên quan đến rối loạn hành vi: người bệnh còn nhận thức thường dễ trầm cảm, trong khi người mất nhận thức có xu hướng kích động và loạn thần.
3.7. Các triệu chứng thần kinh khác
-
Rối loạn giấc ngủ: mất ngủ, ngủ ngắt quãng, thay đổi nhịp sinh học, xuất hiện sớm ngay cả khi chức năng nhận thức còn bảo tồn.
-
Co giật: gặp ở 10–20% trường hợp, thường ở giai đoạn muộn hoặc thể di truyền sớm.
-
Triệu chứng vận động: run, cứng, giật cơ, phản xạ nguyên thủy xuất hiện ở giai đoạn cuối.
-
Rối loạn đại–tiểu tiện: thường gặp ở giai đoạn muộn, biểu hiện tiểu không tự chủ.
3.8. Rối loạn tâm thần và hành vi
Gặp phổ biến ở giai đoạn trung bình đến nặng, thể hiện bằng thờ ơ, giảm giao tiếp, trầm cảm, kích động, hung hăng, đi lang thang. Ở giai đoạn muộn, có thể xuất hiện hoang tưởng, ảo giác hoặc hành vi bạo lực. Các rối loạn này không chỉ làm nặng gánh chăm sóc mà còn ảnh hưởng lớn đến chất lượng sống của bệnh nhân và gia đình.
4. Cận lâm sàng
4.1. Trắc nghiệm thần kinh tâm lý
- Trắc nghiệm thần kinh tâm lý giúp hỗ trợ chẩn đoán và theo dõi tiến triển bệnh, xác định kiểu và mức độ suy giảm nhận thức, qua đó phân biệt các dạng sa sút trí tuệ và định hướng điều trị phù hợp.
- Trắc nghiệm thần kinh tâm lý được chia thành nhóm các trắc nghiệm sàng lọc (Thang đánh giá trạng thái tâm thần tối thiểu – MMSE, MoCA, Mini-Cog...), các trắc nghiệm đánh giá chuyên sâu từng loại chức năng nhận thức, trắc nghiệm đánh giá hành vi tâm thần (NPI), đánh giá hoạt động hàng ngày (ADL, IADL).
4.2. Chẩn đoán hình ảnh
- MRI não: phát hiện teo não toàn thể, teo não khu trú, các tổn thương chất trắng. Tuy nhiên tổn thương đặc trưng nhất là giảm thể tích hồi hải mã và teo thùy thái dương trong.
- FDG-PET/SPECT: giảm chuyển hoá glucose vùng thái dương – đỉnh; PET amyloid hoặc tau cho phép phát hiện tích tụ protein bệnh lý từ giai đoạn tiền lâm sàng.
4.3. Dấu ấn sinh học (Biomarkers)
- Trong dịch não tuỷ (CSF): Aβ42 giảm, t-tau và p-tau tăng, là dấu hiệu sinh học đặc trưng, có độ nhạy và đặc hiệu cao (~85–90%), được coi là tiêu chuẩn vàng trong chẩn đoán sớm.
- Trong huyết tương:
+ Tỷ lệ Aβ42:Aβ40 giảm, p-tau181 hoặc p-tau217 tăng, cùng chuỗi nhẹ sợi thần kinh (Neurofilament light chain -NfL) phản ánh thoái hoá sợi trục thần kinh.
+ Ưu điểm: ít xâm lấn, dễ thực hiện, có thể thực hiện tại cộng đồng; tuy nhiên độ nhạy và đặc hiệu thấp hơn dịch não tuỷ.
4.4. Các xét nghiệm máu giúp chẩn đoán phân biệt
Xét nghiệm vitamin B12 nhằm loại trừ nguyên nhân thiếu vitamin B12, hormon tuyến giáp nhằm loại trừ suy giáp. Đây là những nguyên nhân có thể gây suy giảm nhận thức.
4.5. Xét nghiệm gen
Xét nghiệm gen không được khuyến cáo thực hiện thường quy trong chẩn đoán Alzheimer.
-
Gen APP, PSEN1, PSEN2 chỉ nên xét nghiệm ở các trường hợp sa sút trí tuệ khởi phát sớm có tiền sử gia đình di truyền trội trên nhiễm sắc thể thường.
-
Gen APOE ε4 liên quan nguy cơ cao xuất hiện bất thường hình ảnh học do amyloid (ARIA) ở bệnh nhân dùng thuốc điều trị thay đổi tiến triển bệnh. Vì vậy, nên sàng lọc gen APOE ε4 trước điều trị để phát hiện người bệnh có nguy cơ cao và theo dõi chặt chẽ trong quá trình sử dụng thuốc.
5. Chẩn đoán và chẩn đoán phân biệt
5.1. Chẩn đoán xác định
Chẩn đoán bệnh Alzheimer hiện nay chủ yếu dựa trên tiêu chuẩn DSM-5 (Hiệp hội Tâm thần Hoa Kỳ, 2013) và NIA–AA (Viện Lão khoa Quốc gia Hoa Kỳ và Tổ chức Alzheimer, cập nhật 2021).
- Tiêu chuẩn DSM-5 được áp dụng rộng rãi trong thực hành lâm sàng, tập trung vào đánh giá triệu chứng và khả năng sinh hoạt hàng ngày, trong khi NIA–AA bổ sung các dấu ấn sinh học và phân loại giai đoạn bệnh theo mức độ tiến triển.
Ở những cơ sở có điều kiện xét nghiệm và hình ảnh học hiện đại, tiêu chuẩn NIA–AA được ưu tiên vì phản ánh cách tiếp cận chẩn đoán sinh học hiện nay (Phụ lục)
5.2. Chẩn đoán phân biệt
-
Sa sút trí tuệ mạch máu: tiến triển theo bậc thang, có tổn thương mạch não, suy giảm chức năng điều hành
-
Thể Lewy: dao động nhận thức, ảo thị, triệu chứng Parkinson.
-
Thoái hoá thùy trán – thái dương (FTD): thay đổi hành vi, ngôn ngữ và trí nhớ gặp vấn đề.
-
Giả sa sút trí tuệ do trầm cảm: khí sắc trầm, cải thiện khi điều trị.
-
Sa sút trí tuệ hỗn hợp: kết hợp Alzheimer và bệnh lý mạch máu nhỏ.
6. Điều trị
Hiện chưa có thuốc chữa khỏi bệnh Alzheimer, song các liệu pháp hiện nay có thể làm chậm tiến triển và cải thiện chất lượng sống.
6.1. Điều trị triệu chứng nhận thức
-
Thuốc ức chế cholinesterase (ChEIs): Donepezil, Rivastigmine, Galantamine – tăng acetylcholine, cải thiện trí nhớ và hành vi.
-
Thuốc đối kháng NMDA: Memantine – giảm độc tính glutamate, dùng ở giai đoạn trung bình – nặng, có thể phối hợp ChEIs. Tác dụng phụ thường nhẹ (buồn nôn, nhịp chậm, chóng mặt), giảm khi tăng liều từ từ.
6.2. Thuốc điều trị theo cơ chế bệnh (Disease-Modifying Therapies – DMTs)
Các kháng thể đơn dòng chống amyloid như Aducanumab, Lecanemab, Donanemab được FDA Hoa Kỳ phê duyệt (2021–2024) cho bệnh Alzheimer giai đoạn sớm có bằng chứng amyloid học. Thuốc giúp làm chậm tiến triển nhận thức khoảng 25–35% trong các thử nghiệm lớn, nhưng cần theo dõi biến chứng phù não hoặc vi xuất huyết (ARIA) bằng theo dõi hình ảnh cộng hưởng từ sọ não định kỳ.
6.3. Điều trị rối loạn hành vi và tâm thần
- Trầm cảm, lo âu: dùng thuốc chống trầm cảm nhóm SSRI (Sertraline, Citalopram).
- Kích động, hoang tưởng: thuốc chống loạn thần không điển hình (Risperidone, Quetiapine), liều thấp, thời gian ngắn.
- Rối loạn giấc ngủ: ưu tiên biện pháp không dùng thuốc, điều chỉnh ánh sáng, hạn chế
thuốc an thần.
6.4. Can thiệp không dùng thuốc
- Liệu pháp nhận thức – hành vi, âm nhạc, hồi tưởng (reminiscence therapy) giúp duy trì khả năng nhận thức và giảm kích động.
Thể dục đều đặn (đi bộ, dưỡng sinh, yoga) cải thiện tuần hoàn não, giấc ngủ và tâm trạng.
Dinh dưỡng kiểu Địa Trung Hải: giàu rau, cá, dầu ôliu, hạn chế đường và chất béo bão hoà.
- Hỗ trợ người chăm sóc: hướng dẫn kỹ năng giao tiếp, phòng ngừa kiệt sức và bảo đảm an toàn cho người bệnh.
7. Tiên lượng
Bệnh Alzheimer là bệnh lý thoái hóa thần kinh, tiến triển theo thời gian. Ở giai đoạn muộn của bệnh, bệnh nhân có thể gặp rất nhiều các biến chứng như viêm phổi (do nằm lâu, do hít sặc), chấn thương do té ngã, loét, suy dinh dưỡng và các rối loạn hành vi tâm thần như đi lang thang, kích động, từ chối ăn uống. Các bệnh nhân có biểu hiện suy giảm nhận thức cần được khám và chẩn đoán, điều trị sớm để nâng cao chất lượng cuộc sống và giảm gánh nặng cho người chăm sóc.
TÀI LIỆU THAM KHẢO
1. Tổng cục Thống kê. (2024). Thông cáo báo chí: Kết quả chủ yếu Điều tra Dân số và Nhà ở giữa kỳ năm 2024. Tổng cục Thống kê, Bộ Kế hoạch và Đầu tư.
2. Habib, R., Noureen, N., & Nadeem, N. (2018). Decoding common features of neurodegenerative disorders: From differentially expressed genes to pathways. Current Genomics, 19(4), 300–312. https://doi.org/10.2174/1389202918666171005100549
3. Lamptey, R. N. L., Chaulagain, B., Trivedi, R., et al. (2022). A review of the common neurodegenerative disorders: Current therapeutic approaches and the potential role of nanotherapeutics. International Journal of Molecular Sciences, 23(3), 1851. https://doi.org/10.3390/ijms23031851
4. Gadhave, D. G., Sugandhi, V. V., Jha, S. K., et al. (2024). Neurodegenerative disorders: Mechanisms of degeneration and therapeutic approaches with their clinical relevance. Ageing Research Reviews, 99, 102357. https://doi.org/10.1016/j.arr.2024.102357
5. Saikia, B., & Dhanushkodi, A. (2024). Engineered exosome therapeutics for neurodegenerative diseases. Life Sciences, 356, 123019. https://doi.org/10.1016/j.lfs.2024.123019
6. Scheltens, P., De Strooper, B., Kivipelto, M., et al. (2021). Alzheimer's disease. The Lancet, 397(10284), 1577–1590. https://doi.org/10.1016/S0140-6736(20)32205-4
7. Hội Bệnh Alzheimer và Rối loạn Thần kinh Nhận thức Việt Nam. (2023). Hướng dẫn chẩn đoán và điều trị sa sút trí tuệ 2023.
8. Jack, C. R., Jr., Andrews, J. S., Beach, T. G., et al. (2024). Revised criteria for diagnosis and staging of Alzheimer’s disease: Alzheimer’s Association Workgroup. Alzheimer’s & Dementia, 20(8), 5143–5169. https://doi.org/10.1002/alz.13859
9. Jack, C. R., Jr., Bennett, D. A., Blennow, K., et al. (2018). NIA-AA Research Framework: Toward a biological definition of Alzheimer's disease. Alzheimer's & Dementia, 14(4), 535–562. https://doi.org/10.1016/j.jalz.2018.02.018
10. Zhang, J., Zhang, Y., Wang, J., et al. (2024). Recent advances in Alzheimer's disease: Mechanisms, clinical trials and new drug development strategies. Signal Transduction and Targeted Therapy, 9, 211. https://doi.org/10.1038/s41392-024-01911-3
PHỤ LỤC
1. Tiêu chuẩn của Viện nghiên cứu lão hóa và hiệp hội bệnh Alzheimer (National Institute on Aging and Alzheimer Association) NIA-AA 2011
| Tiêu chuẩn chẩn đoán sa sút trí tuệ |
| Sa sút trí tuệ được chẩn đoán khi có các triệu chứng về nhận thức hoặc hành vi thỏa mãn: 1. Cản trở khả năng làm việc hoặc các hoạt động thường ngày; và 2. Biểu hiện suy giảm so với mức độ hoạt động và làm việc trước đây; và 3. Không do sảng hoặc các rối loạn tâm thần gây ra; 4. Suy giảm nhận thức được phát hiện và chẩn đoán thông qua việc kết hợp của: - Bệnh sử từ bệnh nhân và người chăm sóc hiểu rõ về bệnh nhân - Đánh giá nhận thức khách quan: đánh giá chức năng nhận thức tại giường hoặc trắc nghiệm thần kinh tâm lý (trắc nghiệm thần kinh tâm lý cần được thực hiện nếu hỏi bệnh sử và đánh giá chức năng nhận thức tại giường chưa thể đưa ra chẩn đoán chắc chắn). 5. Suy giảm chức năng nhận thức hoặc hành vi ảnh hưởng đến ít nhất hai trong số các chức năng nhận thức sau: a, Khả năng học tập và ghi nhớ thông tin mới bị suy giảm. Các triệu chứng bao gồm: các câu hỏi và câu chuyện lặp đi lặp lại, thất lạc đồ đạc cá nhân, quên sự kiện hoặc cuộc hẹn, lạc đường trên tuyến đường quen thuộc. b, Giảm khả năng giải thích và xử lý các nhiệm vụ phức tạp, suy giảm khả năng phán đoán. Các triệu chứng bao gồm: giảm khả năng nhận định về rủi ro và tính an toàn, không có khả năng quản lý tài chính, giảm khả năng ra quyết định kém, không có khả năng lập kế hoạch cho các hoạt động phức tạp hoặc tuần tự. c, Chức năng thị giác không gian bị suy giảm. Các triệu chứng bao gồm: không có khả năng nhận diện khuôn mặt hoặc các vật thông thường, không tìm thấy các vật trong tầm nhìn mặc dù thị lực không bị ảnh hưởng, không có khả năng vận hành các dụng cụ đơn giản hoặc mặc quần áo. d, Suy giảm chức năng ngôn ngữ (nói, đọc, viết). Các triệu chứng bao gồm: khó tìm từ khi nói, nói ngập ngừng; lỗi phát âm, lỗi chính tả khi viết e, Thay đổi về tính cách, hành vi hoặc cách cư xử Các triệu chứng bao gồm: những thay đổi tâm trạng bất thường, ví dụ: kích động, giảm động lực, giảm sáng kiến, thờ ơ, thu mình lại, giảm hứng thú với các hoạt động trước đây, mất sự đồng cảm, hành vi ám ảnh hoặc cưỡng chế, hành vi không được xã hội chấp nhận |
| Tiêu chuẩn chẩn đoán có khả năng là bệnh Alzheimer |
| 1. Đáp ứng các tiêu chuẩn sa sút trí tuệ ở mục trên 2. Có các đặc điểm sau: a, Khởi phát âm thầm: Các triệu chứng tiến triển trong nhiều tháng đến nhiều năm, không đột ngột trong vài giờ hoặc vài ngày. b, Tiền sử rõ ràng về suy giảm nhận thức theo thông tin được cung cấp hoặc quan sát c, Loại chức năng nhận thức suy giảm đầu tiên và nổi bật nhất trong quá trình hỏi bệnh và thăm khám thuộc một trong số các chức năng sau: - Biểu hiện trí nhớ: biểu hiện phổ biến nhất của sa sút trí tuệ do bệnh Alzheimer; các triệu chứng khác bao gồm suy giảm khả năng học tập và nhớ lại thông tin mới; kèm theo có bằng chứng về sự suy giảm ở ít nhất một chức năng nhận thức khác. - Biểu hiện ngoài trí nhớ: + Biểu hiện ngôn ngữ: triệu chứng nổi bật nhất là giảm khả năng tìm từ; kèm theo suy giảm các chức năng nhận thức khác + Biểu hiện thị giác không gian: triệu chứng nổi bật nhất là suy giảm nhận thức không gian, bao gồm mất nhận thức về vật thể, giảm khả năng nhận dạng khuôn mặt, mất khả năng nhận thức đồng bộ và mất khả năng đọc; kèm theo suy giảm các chức năng nhận thức khác + Biểu hiện suy giảm chức năng điều hành: triệu chứng nổi bật nhất là suy giảm khả năng lý luận, phán đoán và giải quyết vấn đề; kèm theo suy giảm các chức năng nhận thức khác. 3. Không nên chẩn đoán rất có thể là bệnh Alzheimer khi có các bằng chứng về: a. Bệnh lý mạch máu não đáng kể kèm theo, được xác định bằng tiền sử đột quỵ có liên quan về mặt thời gian với sự khởi phát suy giảm nhận thức hoặc làm cho tình trạng suy giảm nhận thức trở nên trầm trọng hơn; hoặc sự hiện diện của nhồi máu não đa ổ hoặc nhồi máu não lớn hoặc tăng tín hiệu chất trắng nghiêm trọng b. Các đặc điểm nổi bật của Sa sút trí tuệ thể Lewy c. Các đặc điểm nổi bật của Sa sút trí tuệ trán thái dương biến thể hành vi d. Các đặc điểm nổi bật của thất ngôn tiến triển nguyên phát biến thể ngữ nghĩa hoặc thất ngôn tiến triển nguyên phát biến thể không lưu loát e. Bằng chứng về một bệnh thần kinh hoặc bệnh lý ở cơ quan khác hoặc sử dụng thuốc có tác động đáng kể đến nhận thức. |
| Tiêu chuẩn chẩn đoán có thể bệnh Alzheimer |
| 1. Diễn biến không điển hình Diễn biến không điển hình đáp ứng các tiêu chí lâm sàng cốt lõi về loại chức năng nhận thức bị suy giảm đối với sa sút trí tuệ trong bệnh Alzheimer, nhưng có khởi phát đột ngột hoặc minh chứng không đủ chi tiết về bệnh sử hoặc bằng chứng khách quan về tình trạng suy giảm nhận thức tiến triển. Hoặc, 2. Biểu hiện hỗn hợp về nguyên nhân Biểu hiện hỗn hợp về nguyên nhân đáp ứng tất cả các tiêu chí lâm sàng cốt lõi đối với sa sút trí tuệ trong bệnh Alzheimer nhưng có bằng chứng về: (a) bệnh mạch máu não đáng kể đi kèm; hoặc (b) các đặc điểm của sa sút trí tuệ thể Lewy; hoặc (c) bằng chứng về một bệnh thần kinh hoặc bệnh lý ở cơ quan khác hoặc sử dụng thuốc có tác động đáng kể đến nhận thức |
2. Tiêu chuẩn của Hiệp hội Tâm thần Hoa Kỳ, 2013 - DSM-V
| Tiêu chuẩn chẩn đoán sa sút trí tuệ (Rối loạn thần kinh nhận thức nặng theo DSM-V) |
| A. Có bằng chứng suy giảm nhận thức đáng kể ở một hoặc nhiều lĩnh vực nhận thức (sự tập trung chú ý, chức năng điều hành, học tập và trí nhớ, chức năng ngôn ngữ, thị giác không gian và nhận thức xã hội) dựa trên: 1. Than phiền của người bệnh, hoặc của người thân hoặc ghi nhận bởi bác sĩ về sự suy giảm rõ rệt chức năng nhận thức của bệnh nhân 2. Suy giảm đáng kể trong biểu hiện nhận thức, tốt nhất được xác định bởi các trắc nghiệm thần kinh tâm lý đã được chuẩn hóa hoặc nếu không thì dựa trên đánh giá lâm sàng có chất lượng khác. B. Suy giảm nhận thức làm ảnh hưởng đến tính độc lập trong các hoạt động sinh hoạt hàng ngày (tức là cần sự hỗ trợ tối thiểu ở các hoạt động sống phức tạp như trả hóa đơn, dùng thuốc điều trị). C. Bệnh nhân không đang bị mê sảng, lú lẫn cấp D. Suy giảm nhận thức không phải do nguyên nhân tâm thần kinh khác (ví dụ: trầm cảm hoặc tâm thần phân liệt) |
| Tiêu chuẩn chẩn đoán sa sút trí tuệ do bệnh Alzheimer |
| A. Thỏa mãn tiêu chuẩn SSTT B. Suy giảm nhận thức khởi phát từ từ và tiến triển tăng dần ở ít nhất 2 lĩnh vực nhận thức C. Thỏa mãn tiêu chuẩn có khả năng hoặc có thể bệnh Alzheimer dưới dây: Chẩn đoán có khả năng bệnh Alzheimer nếu thỏa mãn một trong hai tiêu chuẩn sau, còn không thỏa mãn thì chẩn đoán có thể bệnh Alzheimer: 1. Bằng chứng có đột biến gen gây bệnh Alzheimer từ tiền sử gia đình hoặc kiểm tra di truyền học 2. Có cả 3 tiêu chuẩn sau: a. Bằng chứng rõ ràng giảm trí nhớ và khả năng học tập và ít nhất một trong các lĩnh vực nhận thức khác (dựa vào hỏi tiền sử và các test thần kinh tâm lý) b. Tiến triển suy giảm nhận thức nặng dần liên tục và từ từ, không có thời kỳ bình nguyên kéo dài c. Không có bằng chứng của các nguyên nhân kết hợp khác (như không có bệnh lý thoái hóa thần kinh khác và các bệnh lý mạch máu não hoặc các rối loạn thần kinh, tâm thần khác hoặc các bệnh lý hệ thống gây suy giảm nhận thức). 3. Những rối loạn này không được giải thích phù hợp hơn bởi các bệnh lý mạch máu não, các bệnh lý thoái hóa thần kinh khác, tác dụng của một chất hoặc các bệnh lý tâm thần, thần kinh hoặc bệnh lý hệ thống khác. |
Cùng chuyên mục

Giá trị dược lý của rau má (Centella asiatica) trong y học cổ truyền và tiềm năng ứng dụng trong chăm sóc sức khỏe hiện đại
10:39 | 07/04/2026 Bài báo Khoa học

Đánh giá sự tuân thủ điều trị của người bệnh tăng huyết áp tại Bệnh viện Y dược cổ truyền Trà Vinh
18:00 | 29/01/2026 Bài báo Khoa học

Phòng và điều trị bệnh sa sút trí nhớ theo Y học Cổ truyền
11:57 | 21/01/2026 Bài báo Khoa học

Phương pháp luyện thiền: hỗ trợ phòng ngừa sa sút trí tuệ và cải thiện trí nhớ
11:56 | 21/01/2026 Bài báo Khoa học
Các tin khác

Kích hoạt não bộ xã hội: Oxytocin, gắn kết và sức khỏe tinh thần cộng đồng
11:56 | 21/01/2026 Bài báo Khoa học

Thiền chánh niệm trong việc cải thiện suy giảm trí nhớ ở người cao tuổi
11:55 | 21/01/2026 Bài báo Khoa học

Những thay đổi cùa cơ thể khi có tuổi và nhu cầu dinh dưỡng ở người có tuổi
11:55 | 21/01/2026 Bài báo Khoa học

10 Cách thức tuyệt vời giúp cải thiện tăng cường trí nhớ
11:55 | 21/01/2026 Bài báo Khoa học

Ứng dụng của thuốc quy tỳ nghi hưng long trong chăm sóc sức khỏe bảo vệ não bộ cho trẻ rối loạn phổ tự kỷ (asd) và tăng động giảm chú ý (adhd)
11:54 | 21/01/2026 Bài báo Khoa học

Tác động của aga trầm hương lên sóng não và trạng Thái thiền trong cơ chế tự chữa lành
01:57 | 20/01/2026 Bài báo Khoa học

Một số thảo dược hỗ trợ điều trị và phục hồi suy giảm trí nhớ
01:39 | 20/01/2026 Bài báo Khoa học

Suy giảm trí nhớ của người cao tuổi: Thực trạng và giải pháp bảo vệ sức khỏe não bộ tăng cường trí nhớ bằng y học cổ truyền
01:21 | 20/01/2026 Bài báo Khoa học




